Loi de Mariotte
![]()
A l'inverse des corps solides ou liquides qui sont incompressibles, les corps gazeux, eux, ont la faculté de pouvoir être comprimés. Ils sont compressibles.
Pour prévenir les accidents et savoir utiliser le matériel, il faut connaître la relation entre Volume et pression.
I MISE EN ÉVIDENCE et LOI
 |
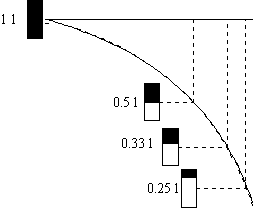
1 * 1 =1
2 * 0.5 =1 3 * 0.33 =1 4 * 0.25 =1 |
 |
|
b) Chaque fois que l'on a multiplié le volume occupé par l'air dans le bocal par la pression absolue qui s'exerce dans le bocal, nous avons toujours obtenue la même valeur P * V = Cte |
Cela signifie que lorsqu'une pression s'exerce sur un gaz, ce gaz occupe un certain volume. Lorsque la pression exercée sur ce gaz augmente, le volume occupé par le gaz diminue d'où la
LOI de MARIOTTE :
A température constante, le volume d'un gaz varie de manière inversement proportionnel à la pression absolue à laquelle il est soumis. P1 * V1 = P2 * V2
II MISE EN APPLICATION EN PLONGÉE
a) la pression absolue sur le volume d'un gaz
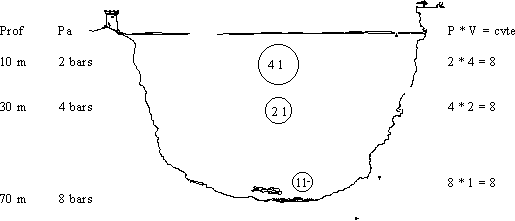
b) Influence de la température
Le dégagement de chaleur n'a pas pour seul effet de réchauffer votre bouteille. En effet, une molécule de gaz qui se réchauffe occupe un volume plus grand, et comme le volume de la bouteille est invariable , c'est donc la pression qui va augmenter
Compléments de thermodynamique
- Équation des gaz parfaits P * V = n R T
- avec:
- P : Pression en pascals (1 bar = 100000 pascals)
- V : Volume en m3
- n : Nombre de moles considérées (1 mole de gaz parfait occupe 22.4 litres à 273°K et à 1 bar)
- R : Constante des gaz parfaits (R = 8.32)
- T : température en kelvin (0°Celsius = 273° kelvin ou T kelvin = T Celsius + 273)
Cas particuliers :
- Pour température constante Loi de Mariotte P x V = Cte (barotraumatismes)
- Pour pression constante Loi de Gay-Lussac V/T = cte (zodiac au soleil)
- Pour volume constant Loi de Chasles P/T = cte (pression avant et après gonflage)
- Tant que le gaz considéré est à une température lointaine de la liquéfaction du gaz, celui-ci se comporte comme un gaz parfait et obéit à la Loi de Mariotte. Comme nous évoluons entre 273° et 303° K, nous disposons toujours de gaz parfaits.
- Nous pouvons simplifier la formule comme cela :
- P * V = n * R * T donc P / T = n * R / V = cte
- dons si P / T = cte on peut écrire P1 / T1 = P2 / T2
Exemple: Une bouteille de 12 l est gonflée à 250 bar à chaud et a une température de 35°C. Quelle sera sa pression intérieure lorsqu'elle sera refroidit à la température ambiante de 25°C ?
D'après la formule précédente, on peut dire : 250 b / 308° k = P2 / 298° k => P2 = 250 * 298° k / 308° k = 241.8 bars
c) Contenance des poumons
Admettons que les poumons contiennent à la surface 6 litres d'air, le plongeur reçoit par son détendeur de l'air à la pression ambiante, c'est à dire à la pression absolue à laquelle se trouve le plongeur.
A 80 m, la pression absolue est de 9 bars. Le volume occupé par un litre d'air est donc 9 fois moins important. Ainsi, à 80 m, le volume d'air dans les poumons est de 9 * 6 = 54 l, volume ramené à la pression atmosphérique au niveau de la mer.
Lors de la remontée, la pression diminuant, l'air va reprendre son volume d'où obligation pour le plongeur de ne pas bloquer sa respiration et d'EXPIRER de manière à laisser échapper l'air et à ne pas soumettre les poumons à une distension appelée SURPRESSION PULMONAIRE.
c) Autonomie du plongeur
- Un plongeur s'immerge avec une bouteille de 12 litres gonflée à 200 bars et ayant une réserve tarée à 30 bars.
- Sachant qu'il respire 16 fois par minute et que chaque inspiration correspond à 1 litre d'air, quelle sera l'autonomie de ce plongeur à 20 mètres, puis à 50 mètres ?
| - Consommation en surface : 16 * 1 = 16 l / mn | |
| - Nombre de litres d'air dans la bouteille : 12 * 200 = 2400 l |
auquel on retire la réserve, car lorsqu'il la passera, il décidera la remontée immédiate
- 12 * 30 = 360 l
- => Air disponible = 2400 - 360 = 2040 l
- - Consommation à 20 mètres pendant 1 mn :
Pa = 3 bars- C = 16 * 3 = 48 litres à la minutes
- En effet, le plongeur inspire à chaque fois 3 litres d'air et non plus 1
- Autonomie à 20 mètres = 2040 / 48 = 42 minutes
- Ou encore P1 * V1 = P2 * V2
- P1 = pression en surface = 1 bar
- V1 = volume d'air disponible = 2040 l
- P2 = pression à 20 mètres = 3 bars
- V2 = volume d'air disponible à 20 m
- => V2 = P1 * V1 / P2 = 2040 / 3 = 680 l
- Si la consommation est de 16 l/mn => A = 680 / 16 = 42 mn
- - Consommation à 50 mètres pendant 1 minute :
- Pa = 6 bars
- C = 16 * 6 = 96 l / mn
- A = 2040 / 96 = 21 minutes
==> Ainsi, plus on descend et plus la plongée est écourtée
d) Flottabilité et équilibrage en profondeur
Lorsque vous êtes équilibré en profondeur à l'aide de la bouée et que vous décidez de remonter, la pression diminuant , le volume de la bouée augmente, accroissant d'autant la Poussée d'Archimède et provocant de ce fait une remontée de plus en plus rapide
==> sachez vous en servir
e) Profondimètre capillaire
Il fonctionne suivant le principe de la Loi de Mariotte. Il est constitué d'un tube de verre ouvert à une extrémité par laquelle l'eau peut rentrer. Plus la pression augmente et plus l'eau rentre dans le tube, l'air s'étend comprimé.
A la moitié de son volume, le tube est gradué 10 m, au quart 30 m...
L'inconvénient de ce profondimètre est que si il est très précis à faible profondeur, il l'est beaucoup moins au delà de 10 m.
Influence de la température :
Si la température de l'eau égale la température de l'air, il n'y a aucun problème
Si la température de l'eau est inférieure à la température de l'air, à la surface de l'eau, l'air contenu dans le tube se refroidit au contacte de l'eau et donc se rétracte. De l'eau pénètre un peu dans le tube et le volume de l'air dans le tube a diminué. A 10 m réel, au lieu que la bulle soit en face de la graduation 10, correspondant à la moitié du volume du tube, elle correspondra à la moitié du volume réduit par le refroidissement. La bulle dépassera donc les 10 m et atteindra 11 ou 12 m.
Si la température de l'eau est supérieure à la température de l'air, à la surface l'air contenu dans le tube se réchauffe au contact de l'eau et donc doit se dilater. Si on s'enfonce immédiatement , cette dilatation va être compensé par la diminution de volume du à l'augmentation de pression. A 10 m réel, la bulle ne sera pas en face de la graduation 10, mais en face d'un chiffre plus faible : ceci est dangereux. Il est donc conseillé de rester quelques minutes à la surface pour que l'air contenu dans le tube se mette à la température de l'eau.
f) Calcul de gonflage
- On a 3 bouteilles tampons de 50 litres chacune et gonflées à 120 b, 150 b et 180 b.
- On a 3 blocs de 12 litres montés en série.
- Il faut toujours prendre la bouteille tampon dont la pression est la plus basse pour terminer par la plus haute ceci quelque soit le volume
- P1 Pression de la bouteille tampon
- V1 Volume de la bouteille tampon
- P2 Pression du bloc
- V2 Volume du bloc
- P3 Pression finale
- 1ère bouteille => (P1 V1) + 3 (P2 V2) = P3 ( V1 + 3 V2)
- => P3 = (P1 V1) + 3 (P2 V2) / V1 + 3 V2 => P3 = (120 * 50) + 3 (1 * 12) / 50 + 3 * 12
- => P3 = 6000 + 36 / 86
- => P3 = 70.18 bars après la 1 ère bouteille tampon
- 2ème bouteille => (P1 V1) + 3 (P2 V2) = P3 ( V1 + 3 V2)
- => P3 = (P1 V1) + 3 (P2 V2) / V1 + 3 V2 => P3 = (150 * 50) + 3 (70 * 12) / 50 + 3 * 12
- => P3 = 7500 + 2520 / 86
- => P3 = 116.51 bars après la 2ème bouteille tampon
- 3ème bouteille => (P1 V1) + 3 (P2 V2) = P3 ( V1 + 3 V2)
- => P3 = (P1 V1) + 3 (P2 V2) / V1 + 3 V2 => P3 = (180 * 50) + 3 (116.5 * 12) / 50 + 3 * 12
- => P3 = 9000 + 4194 / 86
- => P3 = 153.41 bars après la 3ème bouteille tampon
- Gonflage des blocs avec 3 bouteilles tampons montées en série
- (P1 V1) + (P2 V2) + (P3 V3) + 3 (P4 V4) = P5 ( V1 + V2 + V3 + 3 V4 )
- => P5 = (120 * 50) + (150 * 50) + (180 * 50) + 3(1 * 12) / 50 + 50 + 50 + 3 x 12
- => P5 = 6000 + 7500 + 9000 + 36 / 186
- => P5 = 121.16 bars
Il faut donc mieux gonfler des blocs en procédant par équilibrage successifs sur chacune des bouteilles tampons.